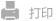乏氧响应的电荷粒径双可变纳米粒用于胰腺癌深部穿透和肿瘤微环境调控
发布时间:2022/6/1 9:20:11 阅读次数:993
近期,本课题组开发了一种用于共递送磷酸化吉西他滨和STAT3抑制剂,以实现化疗药物的胰腺癌深部穿透递送和肿瘤微环境调控的乏氧响应电荷粒径双可变纳米粒。相关研究以Smart Hypoxia-Responsive Transformable and Charge-Reversible Nanoparticles for Deep Penetration and Tumor Microenvironment Modulation of Pancreatic Cancer为题在线发表于国际期刊Biomaterials。

胰腺导管腺癌致密的细胞外基质是阻碍化疗药物递送的主要物理屏障,导致了严重的固有耐药并构建了免疫抑制性的肿瘤微环境。然而,临床上使用紫杉醇白蛋白纳米粒强行破坏胰腺导管腺癌基质屏障的策略会破坏肿瘤细胞与基质组分之间微妙的信号转导和彼此的平衡。这种破坏可能导致肿瘤不受控的生长和转移,使胰腺导管腺癌变的更加难以治疗。
因此,我们设计并构建了一种利用胰腺导管腺癌靶向的核酸适配体GBI-10修饰的乏氧响应纳米颗粒s(DGL)n@Apt用于递送磷酸化吉西他滨和STAT3小分子抑制剂HJC0152。这种纳米粒可以在肿瘤微环境中实现电荷反转,并在乏氧微环境下触发纳米粒的粒径缩小和HJC0152的释放。荷载磷酸化吉西他滨的超小DGL粒子表现了出优异的肿瘤深部穿透、促进化疗药物入胞以及诱导自噬的能力。同时,HJC0152抑制了肿瘤细胞和肿瘤微环境中过度激活的STAT3,可以在保证基质屏障不被完全破坏的基础上软化基质屏障,并将肿瘤微环境塑造为免疫激活状态。此新型共递送策略为胰腺导管腺癌的治疗提供了新的可能性。
课题组2019级直博生陈弘毅为本文第一作者,蒋晨教授为论文的通讯作者。该研究得到了国家自然科学基金委,上海市科技创新行动计划,上海市科技重大专项和张江实验室的支持。
全文链接:https://doi.org/10.1016/j.biomaterials.2022.121599