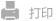DNase I 介导趋化的纳米粒用于急性缺血性脑卒中治疗的 NETs 靶向和微环境重塑
发布时间:2025/6/24 13:13:32 阅读次数:412
中性粒细胞募集和形成中性粒细胞胞外陷阱(NETs)在缺血性卒中再灌注损伤中起重要作用。目前基于纳米药物递送系统的治疗策略主要局限于血脑屏障(BBB)内,忽视了来自外部挑战的持续入侵。考虑到 NETs 独特的血管定位,我们开发了一种 DNase I 介导的NETs靶向纳米粒,整合 DNase I 的催化和趋化功能,实现神经血管单位(NVU)内部和外部微环境的协同调节。 DNase I 将纳米颗粒靶向至病灶部位,通过受损的 BBB 在大脑中积累。清除血管内 NETs 减轻了内皮的持续破坏,减少了免疫血栓的募集。具有双重抗氧化活性的主要纳米颗粒通过清除活性氧(ROS)和保护线粒体挽救神经元凋亡。在小鼠大脑中动脉闭塞/再灌注(MCAO)模型中显示出梗死面积减小和微环境稳态重塑的治疗效果。该策略为缺血性卒中的血管侧治疗提供了新的见解。由酶趋化性介导的靶向性首次得到验证,并展示了通用趋化靶向递送策略的潜力。
相关成果以DNase I-Mediated Chemotactic Nanoparticles for NETs Targeting and Microenvironment Remodeling Treatment of Acute Ischemic Stroke 为题,在线发表于国际知名期刊 Advanced Science(IF=14.1)。

图1 DNase-RM@(PDA/IDB)在脑缺血再灌注损伤中的靶向、反应和治疗机制示意图。
急性缺血性卒中(AIS)是最常见的脑血管疾病之一,死亡率高,致残严重。尽管已经开发了以重组组织纤溶酶原激活剂(rt-PA)为代表的几种溶栓治疗标准,但在临床实践中,严重的继发性缺血再灌注损伤会导致预后不良。最近,越来越多的证据表明中性粒细胞在缺血再灌注损伤中起关键作用。中性粒细胞可迅速募集到病变区域并过度激活形成 NETs。释放的蛋白酶和染色质可能会加剧神经毒性和炎症级联反应。此外,网状 DNA 充当微血栓骨架,捕获其他血细胞并形成免疫血栓形成。NETs 在介导溶栓耐药、加剧缺血再灌注损伤、诱导出血转化和复发方面发挥着不可或缺的作用。
DNase I 被用于降解 NETs,但相关研究仍局限于经典脑靶向给药系统的设计,而忽略了 NETs 区别于其他分子事件的独特生理位置。值得注意的是,缺血性中风不仅是一种脑部疾病,还是一种血管疾病。当关注病变部位神经血管单元(NVU)的血管侧,快速循环的血流环境和较少的可识别异常分子对递送系统的设计提出了新的挑战。
在此,我们提出酶具有成为靶向功能基团的潜力,利用它们的趋化性和底物相互作用可以在特定位点实现富集。具体而言,偶联的 DNase I 用于将纳米粒靶向富含 NETs 的缺血再灌注区域(图1)。通过病灶部位高表达的中性粒细胞弹性蛋白酶(NE)切割释放 DNase I 以降解病理性 NETs,并允许纳米粒通过受损的 BBB 进入大脑进行多靶点治疗。酶的治疗和靶向功能的整合简化了药物递送系统的设计和制备,提高了其疗效和临床转化价值。考虑到 NETs 在炎症和肿瘤等多种疾病发展过程中的重要作用,我们提出的这个策略有望成为一种通用的纳米药物靶向策略。
本课题组博士研究生张童语为论文的第一作者,蒋晨教授为论文的通讯作者。该研究获得国家重点研发计划、国家自然科学基金、上海市科技重大专项、平原实验室公开资助和 ZJLab等项目支持。
原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202503689