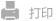由生物启发性脂蛋白引导的工程化智能微环境响应性药物化合物用于逆转肝纤维化
发布时间:2025/3/24 11:06:15 阅读次数:1761
肝纤维化(LF)是一种由多因素引起的进程性慢性疾病,通常以肝星状细胞(HSCs)异常活化、活性氧(ROS)过度积累及细胞外基质沉积为特征。目前,临床尚无FDA获批的抗纤维化药物上市而是聚焦于消除引起肝损伤的相关病因。这种治标不治本的临床治疗策略与有效逆转LF的治疗预期明显矛盾。同时LF的复杂病理机制往往涉及多细胞交互和多信号通路的串扰,导致单药治疗效果有限。因此,我们构建了一种由仿生脂蛋白(sHDL)自导航的微环境响应性前药偶联物共递送平台(PL-VTO),旨在关注疾病的整体微环境互作,开发更高效的多药多靶点协同治疗策略。该共递送平台选用两种可缓解肝纤维化的千层纸素A与视黄醇为模型药物,引入TK键确保两药的体内时空同步协同配合,并利用sHDL封装,赋予其天然的肝脏靶向功能。PL-VTO在克服LF外部屏障的基础上,实现了在病灶部位的高效浓集递送,并可响应高ROS微环境释放出双亲本药物,有效清除ROS,诱导活化HSCs静止,减少胶原沉积,展现出良好的LF治疗潜力。相关成果以Engineered Intelligent Microenvironment Responsive Prodrug Conjugates Navigated by Bioinspired Lipoproteins for Reversing Liver Fibrosis为题,在线发表于国际知名期刊Small Methods (IF=10.7)。
随着纳米技术和生物材料的迅速发展,从自然生物的结构和特性中汲取灵感的仿生设计为更高效的药物递送策略提供了新的可能。sHDL是一种受天然高密度脂蛋白(HDL)结构功能启发而构建的仿生纳米载体。其由磷脂和载脂蛋白模拟肽ApoA-1组成,呈现以冠状结构包裹磷酯而形成的疏水核心结构。通过模拟HDL表面的载脂蛋白ApoA-1,利用其与广泛分布于肝脏表面的SR-B1受体间的高度亲和性,可发挥天然的肝脏靶向药物递送潜能。sHDL不仅具有与天然HDL相似的优良生物相容性、稳定性及肝脏靶向性,还克服了天然HDL提取复杂、难放大生产的困境,是实现输送各种治疗剂至肝脏的理想平台。
合理的前药设计可赋能药物额外的性质和功能,同时也可实现理化性质不同的药物在共递送时的体内药动学行为一致,从而减少随机生物分布,放大协同效应,提高疗效。因此聚焦于LF病灶高ROS微环境特点,引入ROS刺激响应性敏感键将不同药物连接,可实现不同药物在纤维化肝脏的同时同地智能响应性释放。
在此,我们针对LF这种病因复杂、缺乏合理的临床治疗方案的疾病设计开发了一种基于sHDL导航的智能前药偶联物共递送平台(PL-VTO)。与预期相符,所设计的前药偶联物VTO可有效响应ROS断裂并释放出两原型药物,且相比于单一的药物处理,展现出更强大的ROS清除效果。PL-VTO也充分发挥出多药物协同递送与高选择性释放的双重优势,实现了强大的位点特异性积累、高效的ROS清除,和令人满意的LF治疗效果。此外,这种精确的靶向递送和按需的前药激活在整个治疗过程中表现出了良好的安全性。总之,这种精心设计的智能导航双药共递释平台通过整合纳米技术、仿生载体和前药设计等多方优势,不仅解决了LF治疗时的复杂困境,还可为管理其他具有类似复杂病理特征疾病的多药协同治疗提供了可供参考的治疗思路。

本课题组博士研究生方明珠和苏博裕为论文的共同第一作者,孙涛副教授和蒋晨教授为共同通讯作者。该研究获得国家自然科学基金,上海市学术研究带头人计划,平原实验室等项目支持。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/smtd.202402247