针对炎症微环境的ROS清除型纳米药物增强抗癫痫疗效
发布时间:2022/11/24 9:34:49 阅读次数:2669
癫痫是一种以神经元群大规模异常同步放电为特征的脑部疾病。在神经元异常放电之外,更多研究还发现神经胶质细胞增生、氧化应激、炎症反应等病理因素与癫痫发生(Epileptogenesis)有关。在癫痫发生过程中,可能存在某个时间窗,能够抑制大脑中分子、细胞或生理的变化,尤其是神经元损伤和胶质细胞过度激活。病灶发生氧化应激时,炎症反应增强,而清除活性氧(ROS)能够重塑免疫微环境,抑制癫痫发生。因此,抗氧化剂(生物酶、天然化学产物等)和抗癫痫药物的联合使用,可能有助于同步调节炎症微环境和异常神经活动。
但是,通过炎症途径对癫痫发生进行早期干预的策略很少见诸报道。这是因为在递送生物酶和天然化学产物等抗氧化剂时,一方面要克服血脑屏障的阻碍,另一方面在入脑后不能集中分布于癫痫病灶。因此,目前临床上仍然以传统的抗癫痫药(AEDs)作为癫痫的主要治疗手段。但是当前常用的抗癫痫药主要作用于离子通道,无法直接干预氧化应激与炎症反应,因此难以阻断癫痫发生。准确地说,大约30%的癫痫患者对常规抗癫痫药表现出耐受性,最终发展为难治性癫痫。因此,有必要在抗癫痫药之外,引入新的ROS反应性结构。
抗癫痫药的另一大问题,在于其长期用药的潜在副作用,以及停药后癫痫容易复发。这与药物的给药剂量和作用机理有关。第二代抗癫痫药拉莫三嗪(LTG)的副作用比第一代有所降低,但它是一种疏水性药物,限制了其体内有效剂量。为了提高脑部对拉莫三嗪的利用率,同时降低其剂量相关的副作用,本课题组最近报道了一种具有脑靶向递送和ROS响应功能的自组装胶束递药系统。它以苯硼酸酯为两亲分子的疏水端,根据相似相溶原理,包载LTG;以聚乙二醇为亲水端,减少在血液循环过程中网状-内皮系统的吞噬。苯硼酸酯作为ROS响应型敏感基团,在与ROS反应前后,由于亲疏水性改变而促进递药系统解体,释放其中包载的LTG。另外,纳米递药系统的表面还修饰了脱氢抗坏血酸(DHAA,一种葡萄糖类似物),靶向血脑屏障高表达的葡萄糖转运体,借助脑部的高葡萄糖摄取和癫痫病灶的高能量需求而提高入脑效率。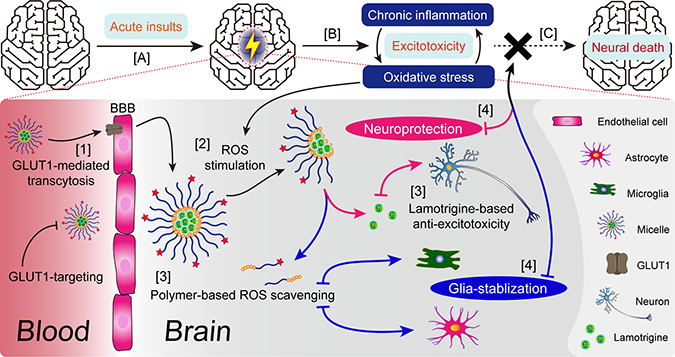
聚合物胶束调节癫痫病灶微环境的示意图
总之,该纳米递药系统一方面能够在DHAA的介导下跨过血脑屏障,并在癫痫病灶高浓度ROS的刺激下解体,释放LTG,抑制神经元的异常放电;另一方面,ROS的清除也阻止了氧化应激和慢性炎症的发展,有助于恢复神经胶质细胞稳态,最终协同发挥抗癫痫疗效。
本课题相关研究成果以“ROS-removing
nano-medicine for navigating inflammatory microenvironment to enhance
anti-epileptic therapy”为题,在线发表于《Acta Pharmaceutica Sinica B》,DOI为10.1016/j.apsb.2022.09.019,即时IF = 14.903。2020级博士研究生周政为第一作者,蒋晨教授为通讯作者。详情请参考https://www.sciencedirect.com/science/article/pii/S2211383522004087。