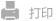通过表观遗传调控抑制癌症干细胞和支持免疫细胞的蛋氨酸分配纳米调节剂
发布时间:2025/2/24 10:11:57 阅读次数:2327
肿瘤的表观遗传失调通过影响基因表达和驱动代谢模式的改变,为其恶性演进、治疗抵抗和形成促瘤的免疫微环境奠定了基础。而这种不受控制的代谢模式又反过来为肿瘤的恶性增殖和表观遗传修饰的可塑性提供了原料保障。近年来,越来越多的研究表明肿瘤通过近似疯狂的方式掠夺营养物质,这一方面满足其自身的能量和物质需求,另一方面也会剥夺免疫细胞获取充足养分的机会。而这种掠夺的能力又离不开失调的表观遗传和基因表达所决定的养分转运体和代谢酶的表达上调,形成了一个紧密相扣的恶性循环。因此,寻找肿瘤代谢和表观遗传的关键连接点可能会为治疗带来机会。针对该连接点的干预,可能同时为破解恶性循环、解除化疗耐药和逆转免疫抑制提供帮助。因此我们设计构建了一种干预肿瘤蛋氨酸摄取并联合免疫原性化疗的共递送纳米调节器(AS-F-NP),其由奥沙利铂前药交联的氟化聚阳离子和靶向蛋氨酸转运体Lat4的siRNA组成,表面经DNA适配体的修饰赋予其肿瘤靶向潜力。AS-F-NP能够通过沉默Lat4限制肿瘤的蛋氨酸掠夺和表观遗传甲基化供体池的可用性,干预肿瘤的表观遗传可塑性并同时恢复微环境中蛋氨酸的水平,进而维持浸润的免疫效应细胞的活力和功能。联合免疫原性化疗,在两种不同的肺转移肿瘤模型中表现出了卓越的激活抗肿瘤免疫和消除癌症干细胞的潜力。相关成果以“A Methionine Allocation Nanoregulator for the Suppression of Cancer Stem Cells and Support to the Immune Cells by Epigenetic Regulation”为题,在线发表于国际知名期刊Advanced Science (1区TOP,IF=14.3)。
表观遗传失调是几乎所有人类癌症的标志性特征,通过直接影响肿瘤细胞的基因表达和表型,驱动其进入异常代谢模式以满足失调的表观遗传的物质需求。表观遗传修饰的动态平衡依赖于可逆修饰特性,这要求肿瘤细胞必须维持充足的代谢原料供应。这种代谢适应性不仅为肿瘤抵抗治疗刺激或向耐药表型转化提供了基础,还通过营养竞争塑造了以"营养匮乏"为特征的肿瘤微环境,导致免疫细胞功能受损。有研究表明,组蛋白/DNA甲基化修饰不仅与肿瘤干细胞表型维持、化疗耐药及转移潜能密切相关,同时也调控CD8+ T细胞等免疫细胞的效应功能,揭示了表观遗传和代谢异常在肿瘤恶性进展中的枢纽作用。
组蛋白/DNA的甲基化修饰所需的活性甲基完全依赖外源性甲硫氨酸供给,这导致肿瘤细胞形成独特的甲硫氨酸成瘾性代谢模式。通过显著上调转运体Lat4的表达,肿瘤细胞在微环境中建立竞争优势,一方面获取充足甲基供体维持表观可塑性,另一方面造成微环境甲硫氨酸耗竭,导致浸润免疫细胞功能紊乱。我们根据患者来源的临床样本和数据库分析,证实了Lat4在肿瘤组织特异性高表达,与免疫抑制微环境的形成显著相关。因此,聚焦于肿瘤细胞的甲硫氨酸成瘾性代谢,既能逆转表观失调相关耐药,又可重塑免疫微环境。然而,由于缺乏针对Lat4的小分子抑制剂,基于siRNA的基因干预成为关键策略,但其疗效高度依赖递送系统的循环稳定性和肿瘤特异性释放能力。
鉴于此,我们开发了交联型氟化聚阳离子/siRNA复合纳米调节器(AS-F-NP),该纳米调节器通过奥沙利铂(OXA)交联氟化低分子量聚乙烯亚胺,实现siRNA的高效包载和稳定递送。其创新性体现在:(1)利用肿瘤细胞内高还原微环境触发药物精准释放和载体降解,避免高分子量的阳离子聚合物的体内蓄积毒性;(2)OXA不仅作为直接杀伤肿瘤的化疗剂,还能通过诱导免疫原性细胞死亡激活抗原呈递细胞启动抗肿瘤免疫应答;(3)siLat4同步抑制肿瘤细胞对甲硫氨酸的过度掠夺,既阻断肿瘤干细胞表型演化增敏化疗,又恢复微环境中免疫细胞的效应功能逆转免疫抑制。最终在两种肺转移肿瘤模型中,该纳米调节器显著抑制了肿瘤进展,为干预肿瘤代谢和表观遗传恶性循环的治疗思路带来了希望。

本课题组博士研究生苏博裕为论文的第一作者,孙涛副教授和蒋晨教授为共同通讯作者。该研究得到了国家自然科学基金委,国家重点研发计划,上海市科技重大专项和张江实验室的支持。
原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202415207